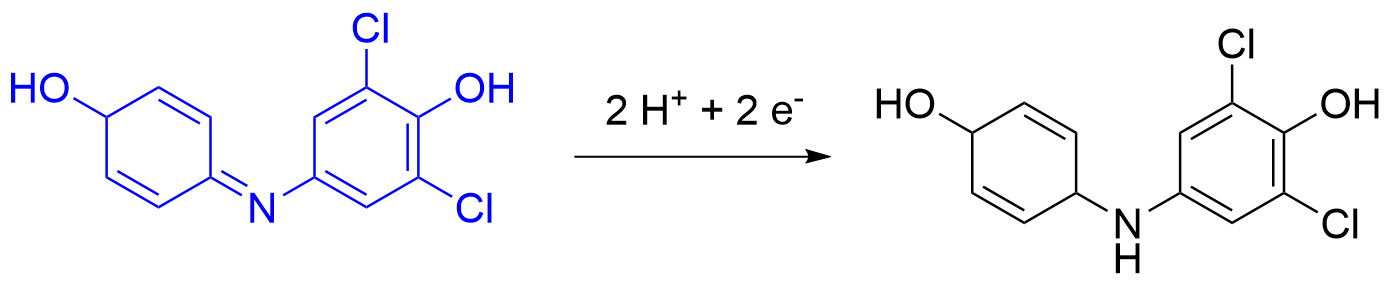Hill-Reaktion mit DCPIP
Allgemeine Hinweise zum Experimentieren und Disclaimer beachten!
Einleitung
Chloroplasten haben die Fähigkeit, unter Einwirkung von Licht, Wasser photolytisch zu H+ Ionen und Sauerstoff zu spalten. Dies kann man in vitro mit einem künstlichen Elektronenakzeptor – auch Hill-Reagenz genannt – nachweisen.
Schwierigkeitsgrad
Schülerexperiment - schwer
Geräte
Frische Blätter, Laborwaage, Wägeschiffchen, 250 mL Becherglas, Standmixer, Lacksieb, Trichter, Falco-Tube 50 mL, Kühlzentrifuge mit passendem Rotor, Pipette 1000 – 5000 µL mit passenden Pipettenspitzen, Reagenzgläser, Halogenscheinwerfer 1000 W, Alufolie, Becherglas 2000 mL, Spatel, Messkolben 500 mL, Eis, Magnetrührer mit Rührfisch (optional), UV/VIS-Spektrometer mit Küvetten (optional).
Chemikalien
Saccharose
Kaliumchlorid
Dinatriumhydrogenphosphat Heptahydrat
Natriumdihydrogenphosphat Monohydrat
2,6-Dichlorphenolindophenol Lösung, wässrig (c = 0.03 %)
Durchführung
Herstellung Extraktionspuffer:
500 mL Extraktionspuffer werden hergestellt aus:
Saccharose: 85.58 g
Kaliumchlorid 0.37 g
Dinatriumhydrogenphosphat Heptahydrat: 3.87 g
Natriumdihydrogenphosphat Monohydrat: 1.46 g
Der Lösevorgang dauert sehr lange, optional kann mit einem Magnetrührer gerührt werden.
Durchführung:
Ein paar frische Löwenzahnblätter o.Ä. werden mit 50 mL Extraktionspuffer (0.5 M Saccharose in 0.05 M Phosphatpuffer + 0.01 M Kaliumchlorid bei pH 7.0) versehen und im Standmixer in kurzen Intervallen (maximal 4 mal 5 s) zerkleinert.
Mittels Filtration durch ein Lacksieb, werden die groben Bestandteile von den feinen Chloroplasten getrennt. Die Filtrationsvorlage ist dabei mit Eis zu kühlen!
Um möglichst viele der unerwünschten löslichen Bestandteile zu entfernen, wird bei 7800 RPM und 4 °C für 5 min zentrifugiert, der Überstand verworfen, mit frischem Extraktionspuffer auf ungefähr das gleiche Volumen aufgefüllt und erneut zentrifugiert. Abschließend wird wieder mit frischem Extraktionspuffer aufgefüllt.
Nun werden vier Reagenzgläser nach folgendem Schema vorbereitet. Ein Reagenzglas (Nr. 4) wird dabei vollständig mit Alufolie umwickelt, um es vor Licht zu schützen:
Reagenzglas 1 (Positivprobe):
Extraktionspuffer: 4 mL
DCPIP (c = 0.03%): 1 mL
Reagenzglas 2 (Hell):
Chloroplasten-Suspension: 2 mL
Extraktionspuffer: 2 mL
DCPIP (c = 0.03%): 1 mL
Reagenzglas 3 (Negativprobe):
Chloroplasten-Suspension: 2 mL
Extraktionspuffer: 3 mL
Reagenzglas 4 (Dunkel):
Chloroplasten-Suspension: 2 mL
Extraktionspuffer: 2 mL
DCPIP (c = 0.03%): 1 mL
Die Reagenzgläser werden dann mittels Halogenscheinwerfer belichtet, wobei zwischen Scheinwerfer und Reagenzgläser ein großes Becherglas mit Wasser gestellt wird, um sämtliche Wärme zu absorbieren. Nach 10 min werden die Reagenzgläser miteinander verglichen.
Um eine quantitative Ausarbeitung zu ermöglichen, kann den Reagenzgläsern 2 und 4 jeweils 1 mL entnommen, die festen Bestandteile durch Zentrifugation entfernt und die Absorption bei 600 nm mittels UV/VIS-Spektrometer gegen Reagenzglas 3 als Referenz gemessen werden. Die Absorption von Reagenzglas 1 wird gegen den Puffer als Referenz gemessen.
Entsorgung
Alle Lösungen, die 2,6-Dichlorphenolindophenol enthalten, müssen als halogenhaltiger Abfall entsorgt werden. Der Extraktionspuffer kann über das Abwasser entsorgt werden.
Erklärung
Während der Photosynthese wird Lichtenergie absorbiert und in chemische Energie umgewandelt. Der erste Schritt ist dabei die Hill-Reaktion, bei der Wasser photolytisch gespalten wird und Sauerstoff entsteht, sowie NADP+ als Elektronenakzeptor zu NADPH reduziert wird.
In vitro kann man das mit einem künstlichen Elektronenakzeptor nachweisen: Isolierte Chloroplasten sind in der Lage DCPIP unter Lichteinwirkung zu reduzieren, wobei reduziertes DCPIP nicht mehr blau, sondern farblos erscheint.
Vergleicht man nun die Absorptionswerte bei 600 nm, dem Extinktionsmaximum von DCPIP, ist ersichtlich, dass die Werte des ersten Reagenzglases (nur DCPIP) und des 4. Reagenzglases (DCPIP + Chloroplasten, dunkel) ähnlich groß sind. Es wurde also - wie erwartet - kaum DCPIP reduziert.
Der Inhalt aus Reagenzglas 2 weist nun eine viel geringere Absorption auf, da hier das DCPIP teilweise reduziert wurde.
Robert Hill gelang es auf diese Weise 1937 nachzuweisen, dass bei der Photosynthese der Sauerstoff durch lichtabhängige Spaltung von Wasser entsteht und nicht wie zuvor vermutet durch Reduktion von Kohlendioxid. Spätere Studien mit isotopenmarkiertem Wasser bestätigten diese Aussage.
Video
Literatur
Hill, Robin. "Oxygen evolved by isolated chloroplasts." Nature 139.3525 (1937): 881-882.
Gefährdungsbeurteilung (Gestis-Stoffdatenbank)
Saccharose (Kein Gefahrstoff nach GHS)
Kaliumchlorid (Kein Gefahrstoff nach GHS)
Dinatriumhydrogenphosphat Heptahydrat (Kein Gefahrstoff nach GHS)
Natriumdihydrogenphosphat Monohydrat (Kein Gefahrstoff nach GHS)
2,6-Dichlorphenolindophenol Lösung, wässrig, c = 0.03 % (Kein Gefahrstoff nach GHS)